Lembar Kerja Peserta Didik LKPD Kimia Larutan Elektrolit dan Non Elektrolit
Gurubagi.com. Berikut ini kami bagikan Lembar Kerja Peserta didik LKPD Kimia materi larutan elektrolit dan non elektrolit.
LKPD Kimia ini untuk membantu peserta didik jenjang SMA SMK dalam melakukan praktikum Kimia pada materi larutan elektrolit dan non elektrolit.
Pembelajaran dengan menggunakan Lembar Kerja Peserta Didik (LKPD) merupakan bagian penting yang tidak dapat dipisahkan dari kegiatan pembelajaran kimia SMA/MA.
LKPD merupakan merupakan metode pembelajaran yang digunakan untuk memberikan keterampilan proses pembelajaran pada peserta didik.
Oleh karena itu, LKPD Kimia ini dapat menunjang keterampilan proses pembelajaran Kimia materi larutan elektrolit dan non elektrolit melalui praktikum.
Ringkasan Materi
Pengertian Larutan Elektrolit dan Non Elektrolit
Larutan elektrolit adalah larutan yang dapat menghantarkan listrik, karena di dalam larutan ini terdapat ion-ion yang dapat bergerak secara bebas.
Ion-ion tersebut yang menghantar arus listrik dalam larutan. Pada saat zat terlarut dilarutkan dalam pelarut, senyawa elektrolit mengalami disosiasi menjadi partikel-partikel bermuatan positif dan negatif.
Partikel-partikel tersebut yang disebut sebagai ion, sehingga dapat diketahui bahwa senyawa elektrolit terbentuk dari ikatan ion.
Baca : Lembar Kerja Peserta Didik LKPD Kimia Materi Larutan Asam Basa
Molekul air yang telah mengionisasi termasuk larutan elektrolit, akan tetapi perlu diketahui bahwa setiap senyawa atau molekul yang terkandung dalam sebuah larutan itu sangat menentukan apakah larutan itu penghantar listrik yang baik atau tidak,
Kekuatan Larutan Elektrolit
Untuk menentukn kekuatan larutan dapat diuji dengan menggunakan alat uji elekrtolit, sehingga dapat dibandngkan dari cahaya lampu pijar dan banyaknya gelembung gas dari elektroda.
1. Larutan Elektrolit Kuat
Suatu larutan dapa dikatakan elektrolit kuat jika dialirkan listrik, maka mampu menghantarkan arus elektron sampai dapat menyalakan lampu dengan terang.
Ciri-ciri larutan elektrolit kuat
- Penghantar arus listrik kuat atau baik
- Terionisasi dengan sempurna
- Tetapan atau derajat ionisasi (α) = 1
- Jika diuji, larutan elektrolit kuat memiliki nyala lampu yang terang dan muncul gelembung gas yang banyak
Contohnya :
- Garam (NaCl, KCl, CuSO4dan KNO3),
- Asam Kuat (HCl, HI, HBr, H2SO4dan HNO3), dan
- Basa Kuat (NaOH, Ca(OH)2, Mg(OH)2dan KOH)
Reaksi penguraian elektrolit kuat ditulis dengan tanda anak panah tunggal ke kanan.
Contoh reaksi elektrolit kuat :
- NaCl (aq)→ Na+ (aq) + Cl– (aq)
- H2SO4(aq) → 2 H+ (aq) + SO4 2- (aq)
- NaOH (aq)→ Na+ (aq) + OH– (aq)
2. Larutan Elektrolit Lemah
Secara singkat, larutan elektrolit kuat hanya mampu menyalakan lampu dengan redup dan tidak terang. Larutan elektrolit lemah tidak terionisasi dengan sempurna atau hanya sebagian saja yang terionisasi.
Ciri-Ciri Larutan Elektrolit Lemah
- Penghantar listrik yang kurang baik atau lemah
- Terionisasi sebagian
- Tetapan atau derajat ionisasi (α) 0< α <1
- Jika diuji, larutan elektrolit lemah nyala lampunya lemah dan muncul gelembung gas yang sedikit.
Contoh Larutan Elektrolit Lemah
- Asam Lemah (HCN, H3PO4, CH3COOH, dan C2O3)
- Basa Lemah (NH4OH, Al(OH3),
- dan Fe(OH)3).
3. Larutan Non Elektrolit
Larutan Non Elektrolit adalah jenis larutan yang tidak dapat menghantarkan arus listrik. Larutan non elektrolit terdiri dari beberapa zat yang terlarut didalam air, akan tetapi tidak terurai menjadi ion atau tidak terionisasi.
Didalam larutannya, zat non elektrolit ini masih seperti molekul yang tidak mempunyai muatan listrik. Itulah sebabnya larutan ini tidak bisa menghantarkan arus listrik.
Ciri-Ciri Larutan Non Elektrolit
- Tidak bisa terionisasi.
- Tidak bisa menghantarkan arus listrik atau isolator.
- Tetapan atau derajat ionisasi (α ). α = 0
- Bila diuji, Larutan Non Elektrolit, tidak menyala dan tidak muncul gelembung gas.
Contoh Larutan Non Elektrolit
- Urea = CO ( NH2 )2
- Glukosa = C6H12O6
- Sukrosa = C12H22O11
- Etanol = C2H2OH
Berikut ini ilustrasi larutan elektrolit dan non elektrolit
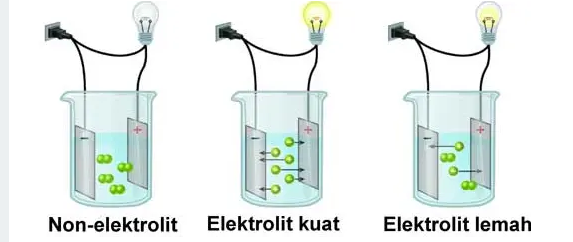
Di bawah ini adalah contoh Lembar Kerja Peserta Didik LKPD Kimia Materi Larutan Elektrolit dan Non Elektrolit.
Lembar Kerja Peserta Didik Larutan Elektrolit dan Non Elektrolit
A. Judul Praktikum
Indentifikasi Larutan Eelektrolit dan Non Elektrolit
B. Tujuan Praktikum
Mengidentifikasi larutan elektrolit dan non elektrolit
C. Alat dan Bahan
- Gelas kimia
- Tisu
- Air secukupnya (pembersih elektroda)
- Baterai berukuran 9 volt
- Kabel listrik
- Bola lampu kecil (usahakan lampu LED 6 volt)
- Elektroda (2 buah paku)
2. Bahan
- Aquades
- Larutan Cuka
- Air gula
- Shampoo
- Air teh
- Alkohol
- Air sumur
- Air jeruk
- Air garam
- Air soda
C. Petunjuk Kerja Praktikum
- Rangkaian alat seperti gambar di bawah ini:

2. Siapkan larutan masukan dalam gelas kimia.
3. Uji larutan dengan cara memasukkan kedua elektroda ke dalam larutan hingga saling bersentuhan.
4. Amati perubahan yang terjadi, apakah lampu menyala redup, tidak menyala atau justru terang.
5. Amati apakah terdapat gelembung, tidak ada atau sedikit.
6. Setelah pengujian selesai dilaksanakan maka larutan akan dibersihkan terlebih dahulu, caranya elektroda yang sudah digunakan dibilas dengan air biasa dan dikeringkan menggunakan tisu.
7. Lakukan hal yang sama untuk larutan berikutnya
8. Amati dengan teliti hingga hasil bisa didapatkan (apakah lampu menyala dan banyaknya gelembung).
Lembar Pengamatan
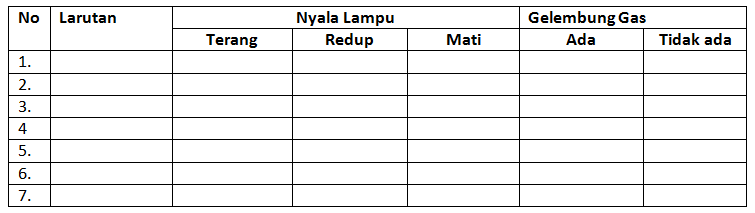
Simpulan :
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
…………………………………………………………………………………………………………………………………………………….
Lembar Kerja Peserta Didik LKPD Kimia materi Larutan elektrolit ddan non elektrolit dalam format PDF dapat di unduh di sini.
Demikian contoh Lembar Kerja Peserta Didik LKPD Kimia materi Larutan elektrolit dan non elektrolit. Semoga bermanfaat.


