Pengertian Kalor, Rumus, Contoh Soal dan Pembahasannya
Gurubagi.com. Di dalam kehidupan sehari-hari pasti sudah tidak asing dengan energi panas atau energi kalor. kalor juga merupakan hal yang sering ditemukan pada mata pelajaran fisika.
Energi kalor ini sebenarnya selalu kita manfaatkan di dalam aktivitas sehari-hari, seperti pada saat kita memasak dan memanaskan suatu benda.
Kalor adalah salah satu bentuk energi yang bisa berpindah dari benda dengan suhu yang lebih tinggi ke benda yang bersuhu lebih rendah jika keduanya dipertemukan atau bersentuhan.
Dengan kata lain kalor adalah salah satu bentuk energi yang bisa diterima atau dilepaskan oleh benda. Saatuan Internasional yang digunakan untuk kalor joule atau kalori.
Dua benda yang memiliki suhu yang berbeda ketika dipertemukan maka akan muncul kalor yang mengalir atau berpindah. Misalnya kita mencampurkan air dingin dengan air panas, kemudian akan menghasilkan air hangat.
Rumus Perhitungan Kalor Perubahan Zat

1. Rumus Perpindahan Kalor
Karena besaran kalor dipengaruhi oleh massa benda, kalor jenis, dan perubahan suhu, maka dapat dirumuskan:
Q = m.c.ΔT
Keterangan:
Q = besaran kalor yang dibutuhkan untuk dilepas atau diterima suatu benda (J)
c = kalor jenis benda atau zat (J/kg⁰C)
m = massa benda atau zat (kg)
ΔT = perubahan suhu (⁰C)
2. Rumus Kalor Jenis
c = Q/m .ΔT
Keterangan:
Q = besaran kalor yang dibutuhkan untuk dilepas atau diterima suatu benda (J)
c = kalor jenis benda atau zat (J/kg⁰C)
m = massa zat atau benda (kg)
ΔT = perubahan suhu (⁰C)
3. Rumus Kapasitas Kalor
C = Q/ΔT
Keterangan:
Q = besaran kalor yang dibutuhkan untuk dilepas atau diterima suatu benda (J)
C = kapasitas kalor (J/K)
ΔT = perubahan suhu (⁰C)
4. Rumus Menentukan Kapasitas Kalor itu Sendiri
C = m.c
Keterangan:
C = kapasitas kalor (J/K)
M = massa zat atau benda (kg)
c = kalor jenis zat atau benda (J/kg.K)
5. Rumus Kalor Lebur dan Uap
a. Kalor Lebur
Q = m.L
b. Kalor uap
Q = m.U
Keterangan:
Q = kalor (J)
m = massa zat atau benda (kg)
L = kalor lebur (J/kg)
U = kalor uap (J/kg)
Baca : Pengertian Suhu, Contoh Soal dan Penerapannya Dalam Kehidupan
Contoh Soal Kalor dan Pembahasannya
Soal nomor 1
Tentukan kalor yang dibuthkan untuk menaikan suhu 0,5 kg zat cair (kalor jenis 400 J/kgoC) dari 28oC menjadi 30oC.
Pembahasan :

Soal nomor 2
Air Sebanyak 2 kg bersuhu 40 oC akan dipanaskan hingga suhu 70 oC. Jika diketahui kalor jenis air 4.186 j/kgoC, Berapakah kalor yang diserap oleh air tersebut?
Pembahasan:
Pada soal ini diketahui:
m = 2 kg
c = 4.186 j/kgoC
∆T = (70 – 40)oC = 30oC
Ditanyakan:
Q = ?
Jawab:
Q = mc∆T
Q = 2 x 4.186 j/kgoC x 30oC
Q = 251.160 J
Soal nomor 3
Air sebanyak 100 gram yang memiliki temperatur 25oC dipanaskan dengan energi sebesar 1.000 kalori. Jika kalor jenis air 1 kal/goC, tentukanlah temperatur air setelah pemanasan tersebut!
Pembahasan:
Diketahui:
m = 100 gram
T0 = 25oC
cair = 1 kal/goC
Q = 1.000 kal
Jawab:
Dengan menggunakan persamaan (3), diperoleh:
Q = mc∆T
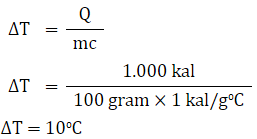
ΔT = T – T0
10°C = T – 25°C
T = 35°C
Jadi, temperatur akhir air setelah pemanasan adalah 35oC.
Soal nomor 4
Tentukan kalor yang digunakan menaikkan suhu 0,1 kg zat cair yang memiliki kalor jenis sebesar 400 J/kg.oC dengan perubahan suhu dari 25oC menjadi 35oC.
Pembahasan:
Diketahui:
m = 0,1 kg
c = 400 J/kg.oC
T1 = 25 oC
T2 = 35 oC
Ditanyakan :
Q =? .
Jawab:
Terlebih dahulu hitung ΔT.
ΔT = T2 – T1 = 35oC – 25oC = 10oC
Menghitung Q
Q = m . c . ΔT = 0,1 kg . 400 J/kg.oC . 10oC = 400 J = 0,4 kJ
Soal nomor 5
Berapakah kalor yang dibutuhkan untuk menaikkan suhu sebuah logam perak yang massanya 8 kg dari 20oC hingga suhu 120 oC. Jika diketahui kalor jenis perak 230 J/kgoC?.
Pembahasan:
Diketahui:
m = 8 kg
T1 = 20oC
T2 = 120 oC
c = 230 J/kgoC
Ditanyakan:
Q = ?
Jawab:
Q = m.c.∆T
Q = m.c. (T2 – T1)
Q = 8 x 230 x 100 oC
Q = 184.000 j = 184 KJ
Jadi, Kalor yang di butuhkan untuk menaikkan suhu logam tersebut yaitu sebanyak 184 KJ
Soal nomor 6
Kalor yang dibutuhkan untuk mengubah suhu 900 gram es dari suhu – 10 oC hingga seluruhnya menjadi air bersuhu 20oC adalah…(kalor jenis air = 1 kal/gr.oC, kalor jenis es = 0,5 kal/gr.oC, kalor lebur es = 80 kal/gr)
Pembahasan:
Diketahui:
m = 900 gram
T1 = – 10 oC
T2 = 20 oC
cair = 1 kal/gr.oC
ces = 0,5 kal/gr.oC
L = 80 kal/gr
Ditanyakan:
Q = …?
Jawab:
Gambaran diagram es menjadi air bersuhu 20oC
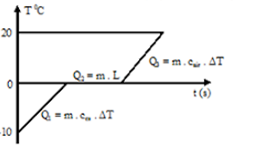
Menghitung Q1
Q1 = m . ces . ΔT = 900 gr. 0,5 kal/gr. C (0 – (– 10)) oC = 4.500 kalori
ΔT = T2 – T1 (suhu tinggi dikurang suhu rendah).
Menghitung Q2
Q2 = m . L = 900 gr . 80 kal/gr = 7.200 kalori
Menghitung Q3
Q3 = m . cair . ΔT = 900 gr . 1 kal/gr.oC (20 – 0)oC = 1.800 kalori
Menghitung Q total
Q = Q1 + Q2 + Q3 = 4.500 kal + 7.200 kal + 1.800 kal = 13.500 kalori
Demikian ulasan mengenai pengertian kalor, rumus, contoh soal dan pembahasannya. Semoga bermafaat
