Penjelasan Golongan A dan B Dalam Tabel Sistem Periodik Unsur
Gurubagi.com. Di dalam sistem periodik unsur, golongan menunjukkan unsur-unsur yang memiliki sifat mirip diletakkan dalam penggolongan.
Golongan dalam tabel periodik unsur terbagi menjadi dua, yaitu golongan A dan golongan B. Golongan A, disebut sebagai golongan utama karena menunjukkan elemen representatif dalam ilmu kimia. Sedangkan golongan B, disebut sebagai golongan transisi.
Untuk menentukan golongan dapat dicari dengan menggunakan konfigurasi melalui jumlah kulit elektron yang terakhir.
Dari konfigurasi elektron tersebut dapat ditentukan letak unsur didalam golongan utama (golongan A) di dalam sistem periodik. Berikut beberapa penamaan khusus golongan.
Baca : Bahan Kimia : Pengertian dan Manfaatnya Bagi kehidupan Manusia
Golongan A
Unsur-unsur pada golongan A merupakan golongan utama. Berikut ini golongan dan unsur-unsur yang terdapat di dalam golongan A
- Golongan IA (alkali, kecuali H), terdiri dari H, Li, Na, K, Rb, Cs, Fr;
Golongan IIA (alkali tanah), terdiri dari Be, Mg, Ca, Sr, Ba, Ra;
Golongan VIIA (halogen), terdiri dari F, Cl, Br, I, At;
Golongan VIIIA (gas mulia), terdiri dari He, Ne, Ar, Kr, Xe, Rn;
Golongan IIIA (boron-aluminium), terdiri dari B, Al, Ga, In, Ti;
Golongan IVA (karbon-silikon), terdiri dari C, Si, Ge, Sn, Pb;
Golongan VA (nitrogen-fosforus), terdiri dari N, P, As, Sb, Bi;
Golongan VIA (oksigen-belerang), terdiri dari O, S, Se, Te, Po;
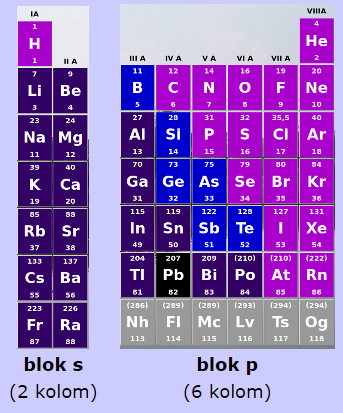
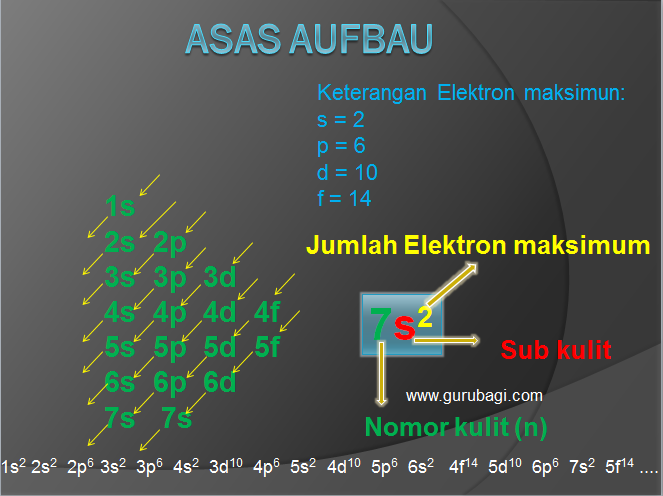
Golongan di dalam konfigurasi elektron diambil dari elektron valensi (elektron pada kulit terluar). Golonga A terdapat dalam blok s-p. Cara menentukan golongan dengan menggunakan konfigurasi elektron.
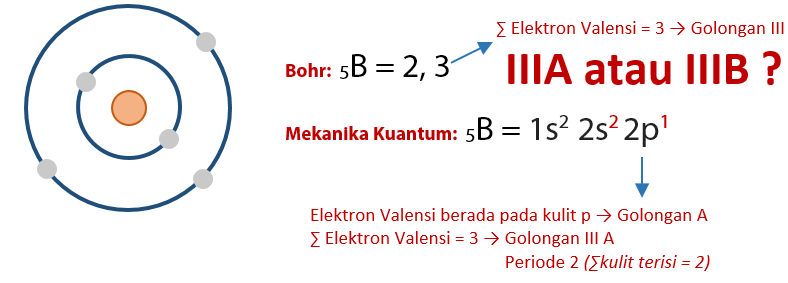
Contoh lain penataan elektron pada golongan A dapat dilihat dari tabel di bawah ini
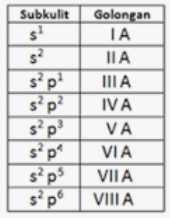
Golongan B
Golongan B adalah unsur-unsur yang berada di blok d,atau unsur-unsur dengan konfigurasi elektronnya berakhir pada kulit d. Di dalam tabel sistem periodik unsur kimia, golongan merupakankolom vertikal.
Golongan B juga dinamakan logam transisi. Dua deret dari bagian bawah merupakan logam transisi dalam yang terdiri atas lanthanide dan aktinida. Golongan IB sampai dengan VIIIB disebut golongan transisi.
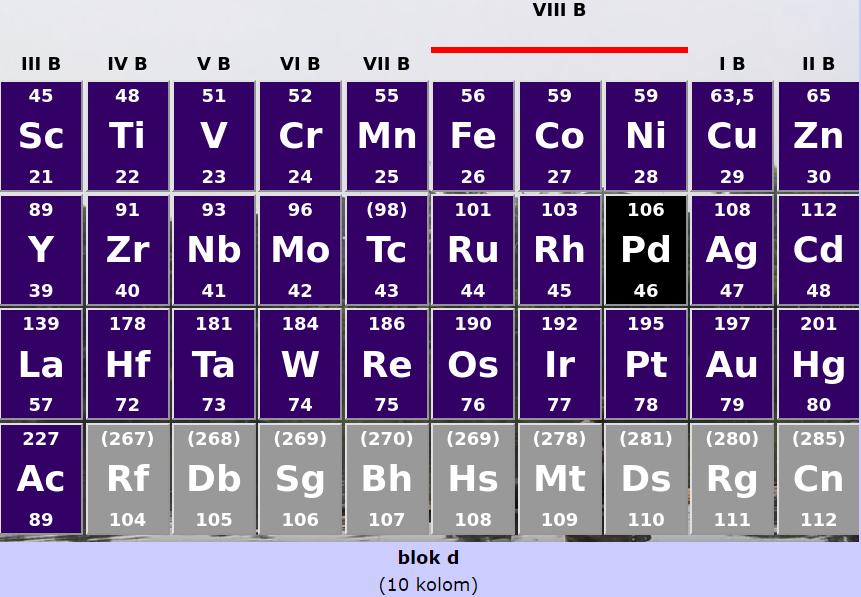
Adapun golongan B memiliki eletron terakhir pada blok s-d. Berikut ini konfigurasi elektron untuk golongan B
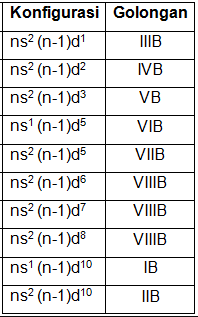
Penentuan golongan B dapat dilihat pada tabel di bawah ini.
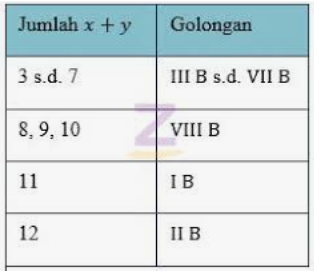
Demikian penjelasan golongan A dan B dalam tabel Sistem Periodik Unsur. Semoga bermanfaat