Sistem Koloid : Pengertian Jenis-jenis dan Sifatnya
Gurubagi.com. Sistem koloid termasuk materi kimia yang dipelajari pada kelas 11, fenomena sistem koloid seing kita jumpai dalam kehidupan sehari-hari, disini akan kita bahas mengenai pengertian koloid,sifat dan contohnya dalam kehidupan sehari-hari.
Koloid adalah jenis campuran heterogen yang terbentuk karena adanya dispersi suatu zat ke dalam zat lain yang dicampurkan, sehingga dalam sistem koloid itu terdapat fase terdispersi dan medium pendispersi.
Fase terdispersi adalah zat yang mengalami penyebaran secara merata dalam suatu zat lain, sedangkan medium pendispersi adalah zat yang menyebabkan terjadinya penyebaran secara merata.
Fase memiliki pengertian berbeda dengan wujud, ada zat yang wujudnya sama, tetapi fasenya berbeda.Contohnya, santan, Perhatikan contoh sistem koloid santan di bawah ini.
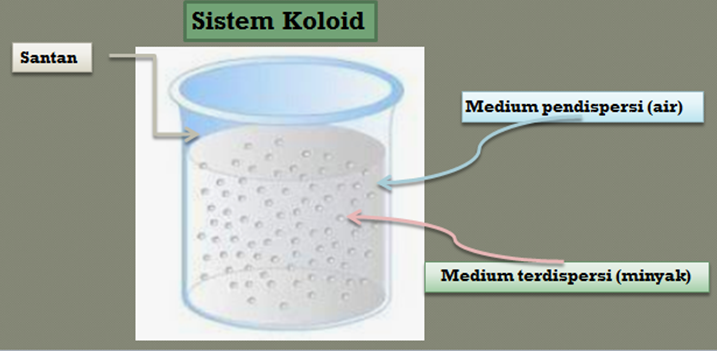
Perhatikan gambar di atas, jika dilihat lebih jelas, dalam larutan santan terdapat butiran minyak dalam air. Butiran minyak tersebut mempunyai fase yang berbeda dengan air, walaupun keduanya berwujud cair.
Butiran minyak dalam santan bertindak sebagai fase terdispersi, sedangkan air sebagai medium pendispersi. Oleh sebab itu, santan juga termasuk contoh sistem koloid yang lain karena punya fase terdispersi dan medium pendispersi.
Ciri-Ciri Koloid
Dari pengertian di atas, untuk lebih jelas mengenal sistem koloid, berikut ini ciri-ciri sistem koloid.
- Terlihat homogen bila dilihat mata, namun berbentuk heterogen bila diamati menggunakan mikroskop ultra.
Terdapat fase terdispersi dan medium pendispersi.
Partikel berdimensi antara 1-100 nm.
Bersifat stabil.
Tidak dapat disaring, kecuali menggunakan alat penyaringan ultra.
Jenis-jenis koloid
Koloid terdiri dari 2 komponen yaitu zat terdispersi dan medium pendispersi. Berdasarkan perbedaan antara fase terdispersi dan medium pendispersi, sistem koloid dibagi menjadi 8, yaitu bisa kita lihat di tabel berikut.
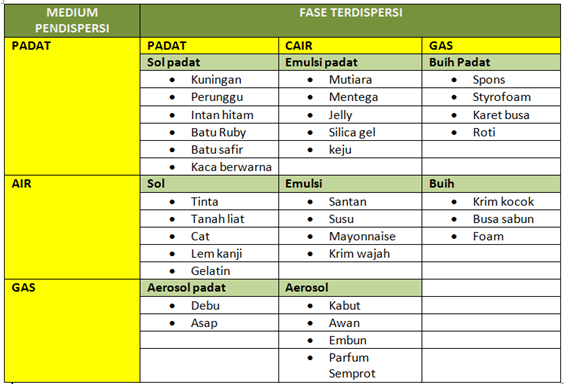
Sifat Koloid
Sifat koloid terbagi mejadi beberapa, diantaranya.
1. Gerak brown (Robert Brown)
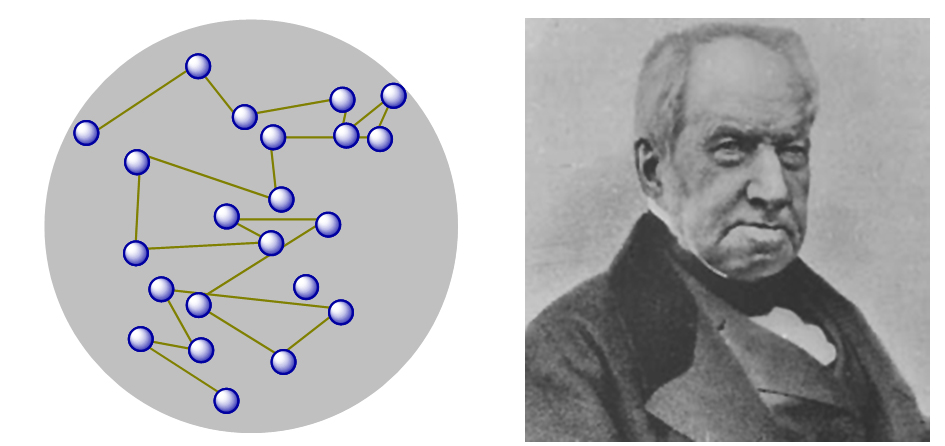
Gerak Brown merupakan gerak acak atau gerak tidak beraturan dari partikel koloid, hal ini dapat kita lihat hanya dengan mikroskop ultra alias tidak bisa kita lihat dengan kasat mata. Partikel ini bergerak acak karena adanya tumbukkan.
Sedangkan pada suspensi tidak ditemukan gerak brown, karena partikelnya terlalu besar, sedangkan pada larutan terjadi gerak brown karena partikelnya kecil, namun tidak dapat teramati dengan mikroskop ultra.
2. Efek tyndall (John Tyndall)

Efek Tyndall merupakan penghamburan cahaya oleh partikel koloid. Partikel dari larutan lebih kecil dari partikel koloid, karena partikel koloid lebih besar dari larutan (partikel larutan < partikel koloid), sehingga berkas cahaya bisa dihamburkan.
Penemuan mengenai efek Tyndall juga dapat menerangkan mengapa langit pada siang hari berwarna biru, sedangkan ketika matahari terbenam di ufuk barat berwarna jingga atau merah.
Ini disebabkan penghamburan cahaya matahari oleh partikel-partikel koloid di angkasa, dan tidak semua frekuensi sinar matahari dihamburkan dengan intensitas yang sama. Hal inilah yang menjelaskan apa yang terjadi pada warna-warna pelangi. John Tynda
3. Adsorpsi
Adsopsi merupakan proses penyerapan, biasa yang diserap itu adalah ion-ion oleh partikel koloid, hal ini terjadi karena luas partikel koloid itu cukup besar sehingga ion-ion itu bisa menempel di permukaan, yaitu ada ion positif dan ion negatif.
Karena koloid mampu menyerap ion-ion maka koloid bisa bermuatan sesuai dengan muatan ion yang diserap. Selama koloid bermuatan, maka koloid ini tidak akan menggumpal karena muatan ion-ion yang sejenis tersebut akan saling tolak menolak.
Misalnya, koloid sol besi (III) hidroksida (Fe(OH)3) yang akan bermuatan positif karena mengadsorpsi ion positif. Sol ini dibuat dengan mencampurkan FeCl3 ke dalam air panas berlebih, sehingga terjadi proses pembentukkan koloid berupa sol hidrat besi (III) oksida atau Fe2O3.xH2O.
FeCl3 + xH2O → Fe2O3.xH2O
Ketika sol Fe(OH)3 terbentuk, ternyata tersisa banyak ion Fe3+ dalam larutan. Ion-ion ini kemudian diserap oleh sol Fe(OH)3 pada bagian permukaannya, yang membuat sol Fe(OH)3 kelebihan muatan positif. Jadi, sol Fe(OH)3 dikenal sebagai koloid bermuatan positif.
4. Koagulasi Koloid

Koagulasi adalah proses rusaknya sistem koloid yang ditandai dengan proses penggumpalan akibat terbentuknya partikel-partikel yang lebih besar ukurannya daripada ukuran koloid (lebih besar dari 100 nm).
Koloid bermuatan jika dihubungkan dengan muatan sejenis akan tolak menolak sehingga tidak akan menggumpal, namun lain halnya, jika muatan koloid di netralkan, sehingga tidak ada lagi tolak menolak, sehingga koloid bisa saling menyatu atau berkelompok sehingga terjadi koagulasi
Koagulasi dapat dipengaruhi oleh pemanasan, pendinginan, penambahan elektrolit, pembusukan, pencampuran koloid yang berbeda muatan, dan elektroforesis.
baca : Power Point PPT Materi Kimia SMA MA Kelas 11
Contoh koagulasi koloid dalam kehidupan sehari-hari, yaitu pada penggumpalan susu yang basi dan telur yang direbus hingga menggumpal atau mengeras bagian putih dan kuningnya.
Demikian Sistem Koloid, Pengertian Jenis-jenis dan Sifatnya. Semoga beranfaat


