Soal Tata Nama Senyawa Kelas 10 SMA SMK Dilengkapi Pembahasannya
Gurubagi.com. Berikut dibagikan soal Tata Nama Senyawa kelas 10 SMA SMK yang dilengkapi dengan pembahasannya.
Soal Tata Nama Senyawa ini untuk membantu belajar peserta didik kelas 10 SMA SMK dalam memahami materi kimia tentang Tata Nama Senyawa.
Tata Nama Senyawa merupakan salah satu materi Kimia yang diajarkan di kelas 10 SMA/SMK, sehingga penting untuk dipahami peserta didik.
Ringkasan Materi Tata Nama Senyawa
Setiap senyawa kimia tentunya memiliki nama spesifik, sehingga dapat dibedakan dari senyawa yang lain. Tata nama senyawa adalah serangkaian aturan persenyawaan-persenyawaan kimia yang disusun secara sistematis.
Seperti halnya penamaan unsur, maka pada mulanya penamaan senyawa didasarkan pada berbagai hal, seperti nama tempat, nama orang, atau sifat tertentu dari senyawa yang bersangkutan.
Di dalam sistem penamaan yang digunakan sekarang, nama senyawa didasarkan pada rumus kimianya.
Seiring perkembangan ilmu pengetahuan, maka tata nama senyawa anorganik dan organik diatur oleh IUPAC (International Union Pure and Applied Chemistry).
Pengaturan tersebut berdasarkan hasil kesepakatan para ilmuwan sedunia, sehingga nama senyawa kimia di seluruh negara sama.
Terdapat dua kelompok besar senyawa yang dikenal saat ini, yaitu senyawa anorganik dan senyawa organik.
Baca : Tata Nama Senyawa Asam Basa Serta Contoh Soal dan Pembahasannya
Tata nama Senyawa anorganik
Berikut adalah yang termasuk senyawa anorganik beserta tatanamanya.
1. Tata nama senyawa ion
Senyawa ion adalah senyawa yang terbentuk dari unsur logam dan nonlogam.
Untuk kation yang hanya punya satu bilangan oksidasi, maka cara penulisannya, yaitu : (nama kation) (nama anion + ida)
Contoh tata nama senyawa ion adalah sebagai berikut.
- NaCl, sehingga disebut Natrium Klorida
K2S , sehingga disebut Kalium Sulfida
Untuk unsur dengan lebih dari satu biloks (beberapa logam gol. IIIA dan beberapa logam transisi gol.B), sehingga cara penulisannya : (nama kation) (bilangan oksidasi kation dalam angka romawi) (nama anion + ida)
Berikut adalah contoh tata nama senyawa yang unsurnya memiliki lebih dari satu bilangan oksidasi.
- Fe2O3, sehingga disebut besi (III) oksida
- Cr2O3, sehingga disebut kromium (III) oksida
2. Senyawa kovalen
Senyawa kovalen adalah senyawa yang dibentuk dari unsur nonlogam dan unsur nonlogam. Di dalam penulisan senyawa jumlah atom penyusun senyawa ditulis dalam bahasa Romawi sebagai berikut.
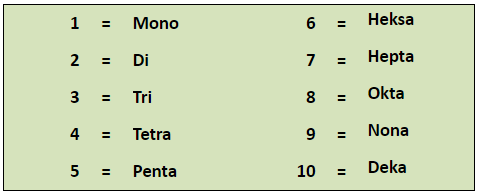
Cara penulisannya, yaitu : (awalan sesuai angka indeks + nama unsur di depan) + ( awalan sesuai angka indeks + nama unsur di belakang + ida )
Berikut adalah contoh nama senyawa kovalen.
- N2O5 = dinitrogen pentaoksida
- PCl5= fosforus pentaklorida
3. Penamaan Senyawa Poliatomik
Senyawa poliatomik adalah senyawa yang tersusun dari banyak atom (lebih dari dua macam atom). Selain itu, sebagian besa senyawa poliatomik memiliki ikatan kovalen dan ionik.
Senyawa poliatomik yang anionnya mengandung oksigen yang lebih sedikit, ditulis dengan awalan hipo-, akhiran –it, sedangkan anion yang mengikat oksigen paling banyak menggunakan awalan per- dengan akhiran –at.
Berikut adalah contoh penamaan senyawa poliatomik.
- NaClO, sehingga dapat ditulis Natrium hipoklorit
- NaClO4, sehingga dapat ditulis Natrium perklorat
3. Tata Nama Asam dan Basa
Tata Nama Asam
Asam merupakan senyawa yang mengandung kation H+ dari suatu anion.
Penulisan tata nama asam, yaitu dengan menyebutkan nama asam + unsur non logam diberi akhiran -ida.
Beikut ini adalah contoh nama senyawa asam.
- HCl = asam klorida
- HBr = asam bromida
Tata Nama Senyawa Basa
Basa adalah senyawa yang didalam larutannya mengandung ion hidroksida(OH-).
Penamaan senyawa asam, yaitu dengan menyebutkan nama senyawa unsur di depan (logam) dan diakhiri dengan hidroksida.
Berikut adalah contoh nama senyawa basa.
- NaOH, sehingga disebut Natrium hidroksida.
- Mg(OH)2, sehingga disebut Magnesium hidroksida.
Soal Tata Nama Senyawa Kelas 10 SMA SMK
Soal Tata Nama Kelas 10 SMA SMK ini berbentuk Pilihan Ganda dengan lima alternatif pilihan jawaban. Di dalam soal sudah dilengkapi kunci jawaban dan pembahasannya, sehingga peserta didik dapat memahami soal yang diberikan.
Soal nomor 1
Rumus kimia yang benar kimia magnesium klorida adalah ….
a. MgCl
b. MgCl2
c. Mg2Cl
d. Mg2Cl2
e. Mg3Cl2
Jawaban : b
Pembahasan :
Di dalam tata nama senyawa ion biner perlu mengetahui berapa jumlah atom penyusunnya. Caranya adalah dengan melihat bilangan oksidasi masing-masing unsur dapat di reaksikan menghasilkan senyawa ion berikut.
Mg = Golongan IIA = Membentuk ion +2 = Mg2+
Cl = Golongan VIIA = Membentuk ion -1 = Cl-1
Mg2+ Cl– → MgCl2
Oleh karena itu jawaban yang tepat adalah MgCl2 (b)
Soal nomor 2
Nama senyawa dengan rumus kimia Li2O yang tepat adalah ….
a. dilitium monoksida
b. dilitium oksida
c. litium oksida
d. litium (I) oksida
e. Litium (II) oksida
Jawaban : c
Pembahasan :
Atom logam 1 = Li = Bilangan oksidasi +1
Atom non logam 2 = O = Oksigen bilangan oksidasi -2, sehingga nama senyawa ion tersebut adalah litium oksida (c)
Soal nomor 3
Nama senyawa Na2O adalah ….
a. Dinatrium oksida
b. Natrium trioksida
c. Natrium pentaoksida
d. Natrium oksida
e. Natrium tetraoksida
Jawaban : d
Pembahasan :
Senyawa oksida diatas termasuk senyawa ion yang mempunyai satu bilangan oksidasi, sehingga pemberian nama dilakukan dengan menyebutkan nama unsurnya yang kemudian dibubuhi kata oksida.
Senyawa Na2O yang tersusun atas unsur Na yang hanya mempunyai bilangan oksidasi +1, oleh karena itu nama yang benar untuk senyawa tersebut adalah Natrium oksida (d).
Soal nomor 4
Diketahui bilangan oksida logam Ca =+2, O= -2, maka nama senyawa yang dibentuk oleh kedua unsur adalah ….
a. Kalsium oksida
b. Kalsium dioksida
c. Kalium oksida
d. Kalium dioksida
e. Kalsium (II) oksida
Jawaban : a
Pembahasan :
Karena Ca‑ + O2- → Ca2O2
Disederhanakan menjadi CaO, sehingga jawaban yang tepat adalah kalsium oksida (a)
Soal nomor 5
Nama senyawa yang tepat untuk Fe2O3 adalah ….
a. Besi oksida
b. Dibesi trioksida
c. Besi dioksida
d. Besi (II) oksida
e. Besi (III) Oksida
Jawaban : e
Pembahasan :
Fe memiliki lebih dari satu bilangan oksidasi, sehingga penamaannya harus diikuti dengan menyebutkan bilangan oksidasinya.
Maka bilangan oksidasi Fe adalah :
2 Fe + 3 O = 0
2Fe+ 3.(-2) = 0
2Fe= +6
Fe = +3
Oleh karena itu nama senyawa tersebut adalah besi (III) oksida (e)
Soal nomor 6
Rumus kimia dari Timah (IV) klorida adalah ….
a. Sn4Cl
b. SnCl4
c. SnCl2
d. SnCl
e. Sn2Cl
Jawaban : b
Pembahasan :
Nama senyawa : Timah (IV) klorida
Timah memiliki bilangan oksidasi +4 = Sn+4
Klorida memiliki bilangan oksidasi -1 = Cl-1
Rumus Kimia Sn4+ + Cl-1→ SnCl4
Oleh karena itu, jawaban yang tepat adalah SnCl4 (b)
Soal nomor 7
Berikut adalah penamaan senyawa yang salah ….
a. NaCl = natrium oksida
b. MgO = Mangnesium oksida
c. AlBr3 = Aluminium bromida
d. ZnS = Seng sulfida
e. FeS = Besi sulfida
Jawaban : e
Pembahasan :
Fe memiliki bilangan oksidasi lebih dari satu, sehingga dalam penulisan senyawanya harus menggunakan angka Romawi dalam tanda kurung.
FeS
X + (-2) = 0
X = +2
FeS : Besi (II) sulfida
Oleh karena itu, jawaban yang tepat adalah FeS : Besi (II) sulfida (e).
Soal no 8
Berikut adalah rumus kimia yang benar untuk aluminium fospat ….
a. AlSO4
b. Al2(SO4)3
c. Al3(SO4)2
d. Al(SO4)2
e. Al(SO4)3
Jawab : b
Pembahasan :
Ion Al memiliki muatan 3+, sedangkan ion poliatomik SO4 memiliki ion 2-
Al3+ + SO42- → Al2(SO4)3, sehingga senyawa tersebut memiliki rumus Al2(SO4)3 (b)
Soal nomor 9
Nama-nama senyawa di bawah ini adalah tidak sesuai dengan rumus kimianya, kecuali….
a. Na2O = Natrium monoksida
b. AlCl3= aluminium trioksida
c. Fe2O3= besi (II) trioksida
d. CaCO3= kalsium karbonat
e. Cu(NO3)2= tembaga nitrat
Jawaban : d
Pembahasan
- Na2O semestinya namanya Natrium Oksida
- AlCl3 semestinya namanya adalah Aluminium klorida
- Fe2O3 semestinya namanya adalah Besi (III) Oksida
- Cu(NO3)2 semestinya namanya adalah Tembaga (II) Nitrat.
Sehingga jawaban yang tepat adalah CaCO3= kalsium karbonat (d)
Soal nomor 10
Nama yang benar untuk senyawa Fe2(SO4)3 adalah ….
a. Besi sulfida
b. Besi sulfida
c. Besi (III) sulfat
d. Besi (II) sulfat
e. Besi sulfat
Jawaban : c
Pembahasan :
Unsur besi memiliki dua jenis ion, yaitu Fe (2+) dan Fe (3+), sementara muatan dari ion sulfat adalah -2.
Senyawa Fe2(SO4)3, angka 3 pada sulfat adalah milik ion lah Fe dan angka 2 pada Fe adalah ion milik sulfat, Fe2(SO4)3 dengan bilangn oksidasi Fe adalah 3, sehingga nama senyawa tersebut adalah besi (III) sulfat (c).
Soal nomor 11
Rumus kimia senyawa difosforus pentaoksida adalah ….
a. 2FO5
b. F2O5
c. 2PO5
d. P2O5
e. 2P2O5
Jawaban : d
Pembahasan :
Berikut adalah penjelasan nama Difosforus pentaoksida
Nama atom logam 1 = fosfor = P , jumlah = di (2)
Nama atom logam 2 = oksigen = O , jumlah = penta (5), sehingga rumus kimia senyawa : P2O5
Oleh karena itu, jawaban yang tepat adalah P2O5 (d).
Soal nomor 12
Rumus kimia yang benar untuk dari senyawa karbon monoksida, yaitu ….
a. CO
b. CO2
c. 2CO
d. C2O
e. CO3
Jawaban : a
Pembahasan :
Karena senyawa poliatom, maka jumlah unsur (1) mono, (2) di, (3) tri dan seterusnya. Atom C berjumlah 1 (mono) dengan akhiran ida, sehingga menurut aturan poliatom rumus senyawa nya CO. Oleh karena itu, jawaban yang tepat adalah CO (a).
Soal nomor 13
Rumus kimia dari senyawa poliatom nitrogen trioksida, yaitu ….
a.NO
b. NO2
c. 2NO
d. N2O
e. NO3
Jawaban : e
Pembahasan :
Karena senyawa poliatom, maka jumlah unsur (1) mono, (2) di, (3) tri dan seterusnya, sehingga jumlah atom N berjumlah 2 = di, dan oksigen 1. Oleh karena itu jawaban yang tepat adalah NO3 (d).
Soal nomor 14
Perhatikan penamaan senyawa berikut!
1). N2O3 = dinitrogen trioksida
2). NO2 = nitrogen oksida
3). N2O5 = dinitrogen pentaoksida
4). N2O = nitrogen tetra oksida
5). NO = nitrogen dioksida
Berikut adalah tata nama senyawa yang benar terdapat pada nomor….
a. 1) dan 2)
b. 1) dan 3)
c. 2) dan 3)
d. 2) dan 4)
e. 2) dan 5)
Jawaban : b
Pembahasan :
Sesuai aturan jumlah atom pada senyawa kovalen bahwa 2 = di, 3 = tri, dan 5 = penta, sehingga N2O5 = N = 2 (di) dan O = 5 (penta), sehingga nama senyawa tersebut dinitrogen penta oksida
N2O3 = N sebanyak 2 (di) dan O sebanyak 3 (tri), sehingga nama senyawa tersebut dinitrogen trioksida. Oleh karena itu, jawaban yang benar adalah nomor (1) dan (3).
Soal nomor 15
Perhatikan tabel berikut!
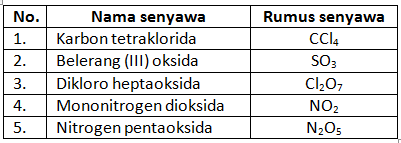
Pasangan nama senyawa dan rumus senyawa yang benar adalah …
a. 1 dan 2
b. 2 dan 3
c. 1 dan 3
d. 3 dan 5
e. 4 dan 5
Jawaban : c
Pembahasan :
Sesuai dengan aturan jumlah atom bahwa jika 1 = mono, 4 = tetra, 2 = di, 7 = hepta, sehingga berlaku untuk senyawa CCl4 dan Cl2O7 karena merupakan senyawa kovalen.
Di dalam CCl4 Jumlah c = 1, jumlah Cl 4 (tetra), sehingga nama senyawa karbon tetraklorida.
Cl2O7 Jumlah Cl = 2(di), O = 7 (hepta, sehingga nama senya dikloro heptaoksida.
Oleh karena itu, jawaban yang tepat adalah 1 dan 3 (c).
Soal nomor 16
Nama yang benar untuk senyawa HNO3 dan H3PO4 adalah ….
a. Asam klorida dan asam nitrit
b. Asam klorida dan asam sulfat
c. Asam posfat dan asam sulfat
d. Asam asetat dan asam cuka
e. Asam nitrat dan asam posfat
Jawaban : e
Pembahasan :
Berikut adalah nama atom H adalah lambang senyawa asam, sedangkan ion poliatomik NO3 = nitrat, PO4 = posfat, sehingga HNO3 = asam nitrat dan H3PO4 = asam posfat. Oleh karena itu, jawaban yang paling teoat adalah asam nitrat dan asam posfat (e).
Soal nomor 17
Berikut definisi yang benar dari pernyataan Bronsted-Lowry mengenai asam adalah ….
a. meningkatkan [H+] bila dalam H2O.
b. menurunkan [H+] bila dalam H2O.
c. meningkatkan [OH–] bila dalam H2O.
d. menerima 1 H+ dari pasangan reaksinya.
e. memberi 1 H+ dari pasangan reaksinya.
Jawaban : e
Pembahasan :
Berikut adalah pernyataan teori asam Brosnted-Lowry.
- Asam: zat yang memberikan 1 H+ pada pasangan reaksinya.
- Basa: zat yang menerima 1 H+ dari pasangan reaksinya.
Oleh karena itu, jawaban yang benar adalah memberikan 1 H+ dari pasangan reaksinya.
Soal nomor 18
Berikut adalah nama yang benar untuk senyawa HCLO4 ….
a. asam perklorat
b. asam sulfat
c. asam klorat
d. asam klorin
e. asam klorida
Jawaban : a
Pembahasan :
H untuk asam dan ClO4 untuk perklorat. Oleh karena itu, nama yang benar adalah asam perklorat (a).
Soal nomor 19
Nama senyawa yang benar untuk NaOH adalah ….
a. Natrium hidroksida
b. Mononatrium hidroksida
c. Natrium oksida
d. Natrium tetraoksida
e. Natrium hidrida
Jawaban : a
Pembahasan :
Na = Natrium,dangkan OH = Hidroksida. ion OH pada basa adalah hidroksida, sehingga nama yang benar untuk NaOH adalah Natrium hidroksida (a).
Soal nomor 20
Nama senyawa yang benar untuk Mg(OH)2 dan Al(OH)3, yaitu ….
a. Mangan hidroksida dan aluminum hidroksida
b. Magnesium hidroksida dan aluminium hidroksida
c. Magnesium hidroksida dan alumunium trihidroksida
d. Mangan dioksida dan aluminuium trihidroksida
e. Magnesium hidroksida dan trialuminum hidroksida
Jawaban : b
Pembahasan :
Berikut adalan nama unsur untuk Mg = magnesium, Al = Aluminium, sedangkan OH merupakan ion hidroksida dari basa.
Nama senyawa yang benar untuk adalah Mg(OH)2 magnesium hidroksida, sedangkan untuk Al(OH)3 adalah aluminium hidroksida.
Oleh karena itu, jawaban yang paling tepat adalah magnesium hidroksida dan aluminium hidroksida (b).
Demikian yang dapat dibagikan mengenai soal Tata Nama Senyawa kelas 10 SMA SMK dan pembahasannya. Semoga bermanfaat.



