Unsur Golongan IIIA, Sifat, dan Kegunaanya
Gurubagi.com. Unsur-unsur yang teradapat di muka bumi ini yang tersusun dengan mudah dalam tabel Sistem Periodik Unsur (SPU), termasuk salah satunya unsur golongan IIIA.
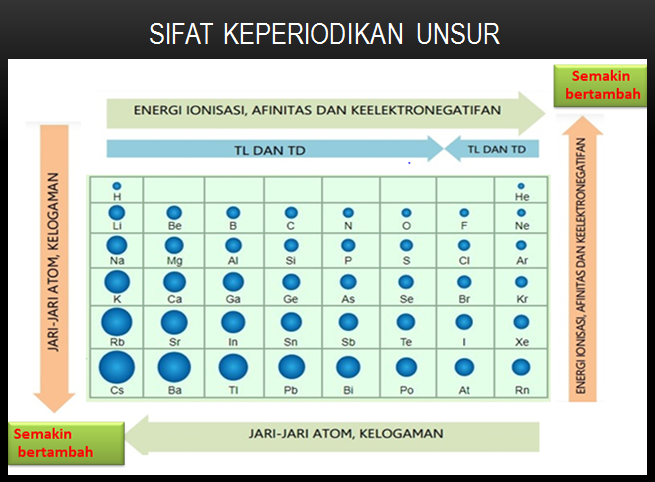
Pada tabel sistem periodik unsur di susun sesuai golongan dan periode. Golongan terdiri atas golongan utama golongan A dan golongan transisi (golongan B).
Unsur golongan A, salah satunya golongan IIIA, merupakan unsur yang akan kita bahas di sini mulai ari pengertian, sifat dan kegunaanya.
Unsur golongan IIIA terletak pada kolom ke-13 pada tabel periodik unsur, sehingga sering disebut sebagai golongan 13. Unsur golongan IIIA terdiri dari baron (B), aluminium (Al), galium (Ga), Indium (In), dan talium (T).
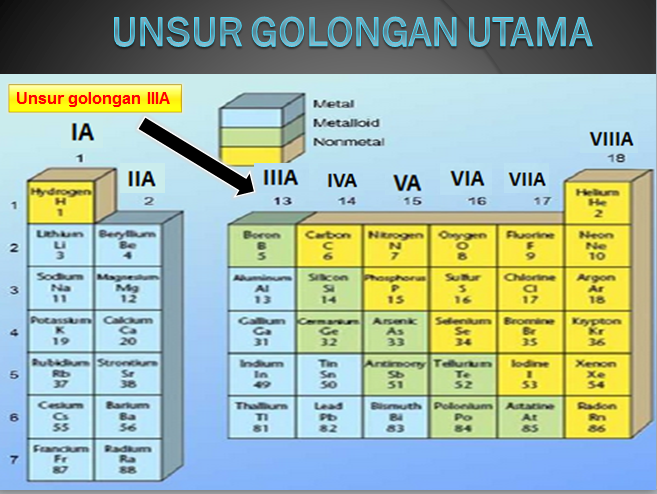
Unsur-unsur pada golongan IIIA mencakup satu unsur non-logam dan empat unsur lainnya yang memiliki sifat kelogaman yang sama.
Unsur-unsur pada golongan IIIA menunjukkan perbedaan sifat yang cukup bervariasi. Berikut ini mengenai unsur golongan IIIA.
1. Boron (B)

Boron merupakan unsur campuran dari logam dan non-logam (metaloid). Boron tidak ditemukan bebas di alam, tetapi dalam bentuk senyawa, sehingg elimpahan boron di alam sangat rendah, sekitar 0,0003%.
Mineral-mineralnya didapatkan dalam bentuk uleksit, boraks, kolemanit, dan kernit. Unsur boron memiliki 2 isotop, yaitu isotop boron-10 denga kelimpahan sekitar 20% dan isotop boron-11 dengan kelimpahan sekitar 80%.
Sifat Fisika dan kimia unsur Boron
a. Sifat fisika
Boron merupakan unsur golongan IIIA yang tergolong metaloid, sedangkan unsur-unsur lainnya tergolong logam. Potensial reduksi golongan IIIA negatif, menunjukkan bahwa unsur IIIA bersifat lebih logam dibanding hidrogen.
Unsur ini juga mempunyai potensial reduksi negatif yang paling besar di antara kation golongan IIIA dan merupakan golongan paling aktif.
b. Sifat kimia
Boron adalah unsur yang tidak relatif pada suhu biasa. Reaksi pada Boron adalah sebagai berikut :
- Reaksi dengan halogen
Boron bereaksi dengan halogen secara umum, bahkan sampai terbakar dalam gas fluor.
2B + 3X2 → 2 BX3
dimana x adalah atom halogen
- Membentuk asam oksi
Jika dipanaskan dalam udara, unsur boron bereaksi dengan oksigen dalam pembakaran yang sangat eksotermik untuk membentuk oksida B2O3 dan sifatnya asam.
B2O3(s) + 3H2O(l) → 2H3BO3(l)
asam borat
Kegunaan Boron
Berikut ini Senyawa boron sedang dievaluasi untuk mengobati arthritis.
a. Senyawa boron digunakan untuk memproduksi kaca borosilikat.
b. Boron nitrida sangat keras, berperilaku sebagai isolator listrik, namun menghantarkan panas, dan memiliki sifat pelumas yang mirip dengan grafit.
c. Boron amorf memberikan warna hijau pada perangkat kembang api.
d. Dapat digunakan sebagai pengendali reaktor nuklir, untuk mendeteksi neutron, dan sebagai perisai radiasi nuklir.
e. Boron dalam magnet NIB (Neodymium – Iron – Boron) digunakan dalam komputer, telepon seluler, peralatan medis, mainan, motor, turbin angin dan sistem audio.
2. Alumunium (Al)
 A
A
AlumuniuAluminium merupakan unsur logam yang berwarna perak menunjukkan banyak kemiripan sifat kimia dengan boron, dan unsur sisanya seluruhnya memiliki karakteristik sebagai unsur logam.
Aluminium adalah logam paling melimpah di dunia dan merupakan unsur ketiga paling umum yang terdiri dari 8% kerak bumi. Fleksibilitas aluminium membuatnya menjadi logam yang paling banyak digunakan setelah baja.
Sifat Alumunium
Sejumlah garam aluminium seperti halnya logam golongan IIIA mengkristal dalam larutannya sebagai hidrat. Perhatikan reaksi berikut :
![]()
Aluminium dapat berlaku asam atau basa dikarenakan kecenderungan yang kuat untuk dioksidasi menjadi Al3+.
Reaksi ini terjadi pada permukaan aluminium yang bersih tetapi dalam larutan asam atau dengan kehadiran basa kuat, lapisan tipis Al(OH)3 ini larut dengan reaksi seperti berikut :
![]()
Kegunaan Alumunium
Beberapa senyawa aluminium yang banyak digunakan dalam kehidupan sehari- hari dan industri, antara lain:
• Tawas, KA(SO4)2.12H2O digunakan untuk mengendapkan kotoran pada penjernihan air.
• Aluminium sulfat Al2(SO4)3 digunakan dalam industri kertas dan mordan (pengikat dalam pencelupan).
• Zeolit Na2O Al2O3.2SiO2 digunakan untuk melunakkan air sadah.
• Aluminium Al2O3 untuk pembuatan aluminium, pasta gigi, industri keramik, dan industri gelas.
3. Galium

Galium yang sangat murni padat merupakan memiliki warna keperakan menakjubkan dan logam ini memuai sebayak 3.1% jika berubah dari bentuk cair ke bentuk padat. Galium tidak terdapat dalam bentuk murni di alam.
Galium sebenarnya lebih berlimpah dari timbal tapi lebih sulit diakses karena tidak terkonsentrasi selektif dalam mineral sehingga persebarannya cenderung luas.
Sifat unsur Galium
a. Galium padat merupakan logam abu-abu kebiruan yang memiliki struktur kristal ortorombik, sedangkan galium murni memiliki warna keperakan.
b. Unsur ini satu dari empat logam: raksa, cesium dan rubidium yang dapat berbentuk cair dekat pada suhu ruangan, sehingga dapat dignakan pada termometer suhu tinggi.
c. Galium padat cukup lunak sehingga bisa dipotong dengan pisau.
d. Galium stabil di udara dan air, tetapi bereaksi dan larut dalam asam dan basa
Kegunaan Unsur Galium
a. Galium paling banyak digunakan dalam bidang elektronika, seperti membuat sirkuit mikrowave dan infrared, semikonduktor dan LED berwarna biru dan ungu.
b. Galium arsenida bisa menghasilkan cahaya laser jika dialiri oleh listrik sehingga bisa digunakan untuk membuat penel surya.
c. Senyawa galium nitrida (GaN) digunakan sebagai semikonduktor dalam teknologi Blu-ray (suatu format DVD yang didesain untuk menyimpan data dan video high definition), smartphone, sensor tekanan untuk teknologi layar sentuh.
d. Galium cair jika dikenakan pada permukaan porselin dan kaca akan membentuk lapisan terang sangat reflektif yang bisa digunakan membuat cermin.
4. Indium (In)

Indium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang In dan nomor atom 49. Unsu indium di kerak bumi jarang berada sebagai butiran logam bebas, terlalu langka dan kecil untuk kepentingan komersial.
Sifat Unsur Indium
a. Sifat Fisika
- Logam berwarna putih-keperakan yang sangat ulet dengan kilau terang.
Sangat lembut seperti natrium, dan bisa dipotong menggunakan pisau.
Meninggalkan garis yang terlihat di atas kertas.
Anggota golongan 13 pada tabel periodik.
Seperti galium, indium mampu membasahi kaca.
6. Memiliki titik leleh rendah, 156,60 °C (313,88 °F); lebih tinggi daripada homolognya yang lebih ringan, galium, tapi lebih rendah daripada homolognya yang lebih berat, thallium, dan lebih rendah daripada timah.
b. Sifat kimia
1. Dalam beberapa kasus, pasangan elektron 5s tidak disumbangkan, menghasilkan In+.
2. Stabilisasi keadaan monovalen terkait dengan efek pasangan inert, di mana efek relativistik menstabilkan orbital 5s, banyak senyawa indium(I) adalah reduktor kuat.
- Indium(I) oksida dan hidroksida bersifat lebih basa, sedangkan indium(III) oksida dan hidroksida bersifat lebih asam.
4. Indium (I) bersifat reduktor kuat karena Indium (1) cenderung mudah mengalami oksidasi menjadi Indium (III) yang lebih stabil dalam bentuk senyawa.
Baca :
- Sifat Unsur Logam Alkali, Kegunaan, dan Kelimpahannya di Alam
- Sifat Unsur Logam Alkali Tanah, Kegunaan, dan Kelimpahannya di Alam
5. Talium (Tl)

Talium merupakan salah satu unsur golongan II yag tidak berwarna dan tidak berbau dalam bentuknya yang murni. Talium adalah logam yang sangat lembut yang bisa dipotong dengan pisau pada suhu kamar
Boron Boron akan bereaksi dengan oksigen, halogen, asam pengoksidasi, dan alkali jika dipanaskan. Senyawa boron bersifat racun.
Sifat Unsur Talium
a. Talium termasuk logam keperakan yang sangat lunak, lunak, berkilau, mencair pada suhu rendah yang memudar di udara menjadi oksida abu-abu kebiruan.
b. Logam dapat dengan mudah dipotong dengan pisau.
c. Jika di larutkan dalam air, terbentuk talium hidroksida yang beracun beracun (TlOH).
d. Talium larut perlahan dalam asam klorida dan asam sulfat encer dan larut dengan cepat dalam asam nitrat.
Kegunaan unsur Talium
Adapaun kegunaan dari unsur talium adalah :
a. Sebagai bahan semikonduktor pada selenium
b. Ssebagai dopant ( meningkatkan) kristal natrium iodida pada peralatan deteksi radiasi gamma seperti pada kilauan alat pendeteksi barang pada mesin hitung di supermarket.
3. Radioaktif talium-201 (waktu paruh 73 jam) digunakan untuk kegunaan diagnosa pada pengobatan inti.
- Talium adalah racun dan digunakan pada racun tikus dan insektisida, tetapi penggunaannya dilarang oleh banyak negara.
Demikian unsur Golongan IIIA, sifat, dan kegunaanya dan kegunaanya. Semoga bermanfaat