Latihan Soal Termokimia Kimia Kelas 11 SMA MA Kurikulum 2013
Gurubagi.com. Berikut ini kami bagikan latihan soal Termokimia Kimia kelas 11 SMA MA Kurikulum 2013 (K13).
Latihan soal termokimia kImia kelas 11 SMA MA ini untuk membantu belajar peserta didik dalam memahami materi kimia tentang termokimia.
Bentuk latihan soal termokimia kimia kelas 11 SMA/MA ini adalah Pilihan Ganda dengan lima alternatif jawaban dan sudah tersedia kunci jawabannya yang dapat di unduh dengan mudah.

Soal nomor 1
Reaksi penyerapan kalor dari lingkungan ke sistem disebut reaksi ….
A. eksoterm
B. endoterm
C. kimia
D. pembakaran
E. oksidasi
Soal nomor 2
Pada reaksi antara soda api dan HCl, jika kita pegang maka wadah reaksi akan terasa panas. Peristiwa tersebut termasuk contoh reaksi ….
A. endoterm
B. eksoterm
C. isoterm
D. redoks
E. pembakaran
Baca : Persamaan Termokimia, Perubahan Entalpi Standar dan Contoh Soalnya
Soal nomor 3
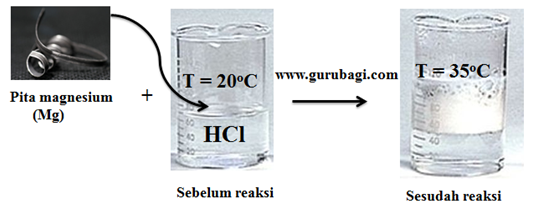
Jika satu sendok serbuk seng dimasukkan ke dalam gelas kimia yang berisi larutan HCl, ternyata terbentuk gelembung gas dan dasar tabung terasa panas. Reaksi ini dapat digolongkan ….
A. eksoterm, energi berpindah dari sistem ke lingkungan
B. eksoterm, energi berpindah dari lingkungan ke sistem
C. endoterm, energi berpindah dari lingkungan ke sistem
D. edoterm, energi berpindah dari sistem ke lingkungan
E. endoterm, energi tidak berubah
Soal nomor 4
Jika diketahui : N2(g) + 3H2(g) → 2NH3(g) ∆H = – 92 kJ, maka perubahan entalpi untuk penguraian 1 mol gas NH3 menjadi unsur-unsurnya adalah ….
A. -92 kJ/mol
B. -46 kJ/mol
C. +46 kJ/mol
D. +92 kJ/mol
E. +184 kJ/mol
Soal nomor 5

Siklus suatu reaksi ditunjukkan dengan diagram di atas mempunyai harga ∆H1 adalah ….
A. -225 kJ
B. +105 kJ
C. -135 kJ
D. +225 kJ
E. -105 kJ
Soal nomor 6
Diketahui :
2NO(g) + O2(g) –> N2O4(g) ΔH = a kJ
NO(g) + O2(g) –> NO2(g) ΔH = b kJ
Besarnya ΔH untuk reaksi : 2NO2(g) –> N2O4(g) adalah ….
A. (a + B) kJ
B. (a – 2B) kJ
C. (a + 2B) kJ
D. (2a + B) kJ
E. (-a + 2B) kJ
Soal nomor 7
Apabila diketahui energi ikatan rata-rata :
N – H = 391 kJ/mol
H – H = 435 kJ/mol
N ≡ N = 946 kJ/mol
maka entalpi pembentukan gas NH3 menurut reaksi : 1/2 N2(g) + 3/2 H2(g) → NH3(g) adalah ….
A. -95 kJ/mol
B. -47,5 kJ/mol
C. 95 kJ/mol
D. 47,5 kJ/mol
E. 50 kJ/mol
Soal nomor 8
Berdasarkan reaksi : H2 + CI2 → 2HCI ∆H = -112 kJ/mol, dapat dinyatakan bahwa pada penguraian 1 mol HCI kalor reaksinya ….
A. endoterm, 56 kJ
B. endoterm, 112 kJ
C. eksoterm, 56 kJ
D. eksoterm, 112 kJ
E. eksoterm, 224 kJ
Soal nomor 9
Jika kalor jenis air adalah 4,18 J.g-1.ºC, maka untuk memanaskan 50 gram air dari suhu 25ºC menjadi 75ºC memerlukan kalor sebesar ….
A. 8,250 kJ
B. 9,725 kJ
C. 10,450 kJ
D. 11,725 kJ
E. 12,45 kJ
Soal nomor 10
Berikut ini yang merupakan reaksi pembentukan standar adalah ….
A. Ca(s) + O(g) + H(g) ——> Ca(OH)2 (s) ΔH = -a kal
B. Ca2+(s) + O2(g) + H2(g) ——> Ca(OH)2 (s) ΔH = -a kal
C. Ca(s) + O2(g) + H2(g) ——> Ca(OH)2 (s) ΔH = -a kal
D. Ca(s) + 2O2(g) + 2H(g) ——> Ca(OH)2 (s) ΔH = -a kal
E. 2Ca(s) + O2(g) + H2(g) ——> 2Ca(OH)2 (s) ΔH = -a kal
Soal nomor 11
Perhatikan persamaan reaksi termokimia di bawah ini :
1. ½ N2 (g) + ½ O2 (g) → NO (g) ΔH = +kJ/mol
2. NO2 (g) → ½ N2 (g) + O2 (g) ΔH = −kJ/mol
3. CO2 (g) → C (s) + O2 (g) ΔH = +kJ/mol
4. C2H5OH + 3O2 → 2CO2 + 3H2O ΔH = −kJ/mol
5. Na(s) + ½ Cl2 (g) → NaCl ΔH = − kJ/mol
Pasangan persamaan reaksi yang merupakan ΔHfº, ΔHdº, dan ΔHcº adalah ….
A. (3), (4), dan (5)
B. (2), (4), dan (5)
C. (1), (3), dan (5)
D. (1), (2), dan (4)
E. (1), (2), dan (3)
Soal nomor 12
Peristiwa berikut ini yang disertai perpindahan kalor dari lingkungan ke sistem adalah ….
A. lilin terbakar
B. campuran kapur tohor dengan air
C. air mendidih
D. petasan meledak
E. minyak goreng membeku
Soal nomor 13
Perhatikan reaksi berikut NO + O2 → NO2. Reaksi tersebut adalah reaksi ….
A. pembentukan NO2
B. pembentukan NO
C. pembakaran NO
D. pembakaran NO2
E. penguraian NO2
Soal nomor 14
Apabila satu molekul air terurai menjadi unsur-unsurnya hidrogen dan oksigen dalam keadaan standar. Pernyataan ini sesuai dengan reaksi ….
A. pembentukan standar
B. penetralan standar
C. penguraian standar
D. pembakaran standar
E. semua jawaban benar
Soal nomor 15
Apabila satu molekul air terurai menjadi unsur-unsurnya hidrogen dan oksigen dalam keadaan standar. Pernyataan ini sesuai dengan reaksi ….
A. pembentukan standar
B. penetralan standar
C. penguraian standar
D. pembakaran standar
E. semua jawaban benar
Soal nomor 16
∆Hfo H2O : -242 kJ/mol
∆Hfo CO2 : -394 kJ/mol
∆Hfo C2H2 : +52 kJ/mol
Jika 5,2 gram C2H2 dibakar secara sempurna sesuai dengan persamaan :
2C2H2 + 5O2 → 4CO2 + 2H2O akan menghasilkan kalor sebesar …. (Ar C = 12; H = 1)
A. 216,4 kJ
B. 432 kJ
C. 1.082 kJ
D. 2.164 kJ
E. 4.328 kJ
Soal nomor 17
Berdasarkan diagram berikut, harga ∆H3 adalah ….

A. ∆H1 + ∆H2 – ∆H4
B. ∆H1 – ∆H2 – ∆H4
C. ∆H2 + ∆H4 – ∆H1
D. ∆H1 + ∆H4 – ∆H2
E. ∆H1 – ∆H2 + ∆H4
Soal nomor 18
Apabila diketahui energi ikatan rata-rata :
N-H = 391 kJ/mol
H-H = 435 kJ/mol
N≡N = 946 kJ/mol,
Entalpi pembentukan gas NH3 menurut reaksi :1/2 N2(g) + 3/2 H2(g) → NH3(g) adalah….
A. – 95 kJ/mol
B. – 47,5 kJ/mol
C. 95 kJ/mol
D. 47,5 kJ/mol
E. 50 kJ/mol
Soal nomor 19
Berdasarkan reaksi : H2 + CI2 → 2HCI ∆H = -112 kJ/mol, dapat dinyatakan bahwa pada penguraian 1 mol HCI kalor reaksinya ….
A. endoterm, 56 kJ
B. endoterm, 112 kJ
C. eksoterm, 56 kJ
D. eksoterm, 112 kJ
E. eksoterm, 224 kJ
Soal nomor 20
Berdasarkan reaksi :H2 + CI2 → 2HCI ∆H = -112 kJ/mol. Dapat dinyatakan bahwa pada penguraian 1 mol HCI kalor reaksinya ….
A. endoterm, 56 kJ
B. endoterm, 112 kJ
C. eksoterm, 56 kJ
D. eksoterm, 112 kJ
E. eksoterm, 224 kJ
Kunci Jawaban – Unduh
Demikian yang dapat kami bagikan Latihan Soal Termokimia Kimia Kelas 11 SMA MA Kurikulum 2013. Semoga bermanfaat.