Soal Penilaian Akhir Semester PAS Kimia Kelas 11 K13 SMA MA 2021
Gurubagi.com. Berikut ini kami bagikan latihan soal Penilaian Akhir Semester PAS Kimia kelas 11 SMA/MA K13 Tahun Pelajaran 2021/2022.
Latihan Soal PAS Kimia kelas 11 SMA MA Kurikulum 2013 ini untuk membantu belajar peserta didik dalam menghadapi Penilaian Akhir Semester PAS Tahun Pelajaran 2021/2022.
Materi soal Penilaian Akhir Semester ini diambilkan dari materi Kimia semester 1 Kelas 11 SMA/MA Kurikulum 2013 (K13).
Baca : Latihan Soal PTS 1 Kimia Kelas 11 SMA K13 Tahun Pelajaran 2021/2022
Materi soal Penilaian Akhir Semester Kimia Kelas 11 SMA/MA Kurikulum 2013 terbagi ke dalam lima bab, sebagai berikut.
Bab 1 Senyawa Hidrokarbon
Bab 2 Minyak Bumi
Bab 3 Termokimia
Bab 4 Laju Reaksi
Bab 5 Kesetimbangan Kimia

Contoh Soal PAS Kimia kelas 11 SMA/MA K13 ini berbentuk pilihan ganda dengan lima alternatif jawaban dan dilengkapi kunci jawaban yang dapat di unduh dengan mudah.
Berikut adalah bentuk latihan soal PAS Kimia kelas 11 SMA MA Kurikulum 2013 tahun pelajaran 2021/2022.
Soal nomor 1
Diketahui beberapa sifat kimia, sebagai berikut.
(1) Sukar larut dalam air
(2) Atomnya hanya dapat disubstitusi oleh halogen
(3) Dapat dijadikan bahan bakar
(4) Ikatannya tak jenuh
(5) Rumus umumnya CnH2n+2
Sifat alkana ditunjukkan oleh nomor ….
A. (1), (2), (3), dan (4)
B. (1), (2), (3), dan (5)
C. (1), (2), (4), dan (5)
D. (1), (3), (4), dan (5)
E. (2), (3), (4), dan (5)
Soal nomor 2
Pada pembakaran sempurna hidrokarbon menghasilkan zat-zat ….
A. CO
B. CO2
C. H2O
D. NO2
E. CO2 dan H2O
Soal nomor 3
Senyawa berikut yang dapat diramalkan memiliki titik didih tertinggi adalah ….
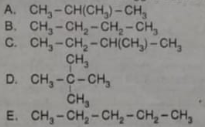
Soal nomor 4
Senyawa dengan rumus (CH3)2CHCH3 mempunyai nama ….
A. butana
B. 2 – metil butana
C. 2 – metil propana
D. pentana
E. propana
Soal nomor 5
Nama senyawa alkana berikut yang benar adalah ….
A. 6 – metil – 4 – propil heptana
B. 2,4,4 – trimetil pentana
C. 2,4,5 – trimetik heksana
D. 4 – etil – 3 – metil heksana
E. 3,4 – dimetil heksana
Soal nomor 6
Perhatikan reaksi berikut!
CH3CH3 + Br2 –> CH3CH2Br + HBr
Reaksi di atas merupakan jenis reaksi ….
A. substitusi
B. eliminasi
C. oksidasi
D. reduksi
E. pembakaran
Soal nomor 7
Minyak bumi yang memiliki titik didih paling rendah adalah ….
A. LPG
B. bensin
C. solar
D. pelumas
E. aspal
Soal nomor 8
Komponen utama bensin adalah ….
A. metana dan etana
B. metana dan butana
C. butana dan heptana
D. heptana dan isooktana
E. oktana dan isooktana
Soal nomor 9
Diketahui beberap zat berikut!
(1) LPG
(2) Bensin
(3) Solar
(4) Alkohol
(5) Kerosin
Hasil fraksi minyak bumi ditunjukkan oleh nomor ….
A. (1), (2), (3), dan (4)
B. (1), (3), (4), dan (5)
C. (1), (2), (3), dan (5)
D. (1), (2), (4), dan (5)
E. (2), (3), (4), dan (5)
Soal nomor 10
Pemisahan fraksi-fraksi minyak bumi dilakukan dengan cara ….
A. kromatografi
B. kristalisasi
C. filtrasi
D. sublimasi
E. distilasi
Soal nomor 11
Mutu bensin dinyatakan dengan angka oktan. Senyawa karbon yang mempunyai angka oktan 100 adalah ….
A.isooktana
B. n – butana
C. n – heptana
D. tetraetil timbal (IV)
E. nafta
Soal nomor 12
Untuk menaikkan mutu bensin, dapat dilakukan dengan menambahkan suatu zat tertentu dalam jumlah relatif sedikit. Zat tersebut adalah ….
A. LNG
B. avtur
C. 2,2,3 – trimetil pentana
D. Pb(C2H5)4
E. isooktana
Soal nomor 13
Di dalam kalorimeter yang telah dikalibrasi dan terbuka, direaksikan 50 g alkohol dan 3 g logam natrium. Jika suhu awal campuran 30ºC dan setelah reaksi suhunya 75ºC, maka nilai ΔHreaksi adalah …. (Clarutan = 3,65 J/gºC, Clarutan = 3,65 J/gºC, ΔTkalorimeter = 10ºC)
A. 8,725 kJ
B. 9,356 kJ
C. -10,205 kJ
D. -12,456 kJ
E. -23,435 kJ
Soal nomor 14
Kalor yang diperlukan untuk menaikkan suhu 50 g air dari 25ºC menjadi 60ºC adalah ….
A. 7,315 kJ
B. 8,872 kJ
C. 9,548 kJ
D. 10,928 kJ
E. 12,987 kJ
Soal nomor 15
Diketahui :
| H2 + F2 –> 2HF | ΔH = -537 kJ |
| C + 2F –> CF4 | ΔH = -680 kJ |
| 2C + 2H2 –> C2H4 | ΔH = 52,3 kJ |
Harga perubahan entalpi untuk reaksi : C2H4 + 6F2 –> 2CF4 + 4HF adalah ….
A. +1.345,5 kJ
B. +2.873,2 kJ
C. -2.468,3 kJ
D. -3.765,2 kJ
E. -6.987,2 kJ
Soal nomor 16
Berdasarkan reaksi : 2NO(g) + 2H2(g) –> N2(g) + 2H2O(g) diperoleh data sebagai berikut.
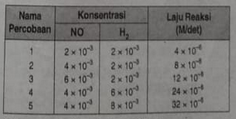
Orde reaksi di atas adalah ….
A. 1
B. 2
C. 3
D. 4
E. 5
Soal nomor 17
Laju reaksi 2P + 3Q2 –> P2Q3 dapat dinyatakan sebagai ….
A. penambahan konsentrasi P, O2, dan PQ3 tiap satuan waktu
B. penambahan konsentrasi P tiap satuan waktu
C. penambahan konsentrasi O2 tiap satuan waktu
D. penambahan konsentrasi PQ3 tiap satuan waktu
E. penambahan konsentrasi P dan O2 tiap satuan waktu
Soal nomor 18
Berikut ini tabel data laju reaksi 2NO(g) + Br2(g) –> 2NOBr(g) pada berbagai konsentrasi.
Rumus laju reaksinya adalah ….
A. v =k[NO2] [Br2]2
B. v =k[NO] [Br2]
C. v =k[NO2]2
D. v =k[NO]2 [Br2]2
Soal nomor 19
Kenaikan suhu dapat mempercepat kecepatan reaksi, karena kenaikan suhu akan ….
A. mempercepat energi kinetik molekul pereaksi
B. memperbesar tekanan molekul pereaksi
C. memperkecil energi pengaktifan zat yang bereaksi
D. memperbesar konsentrasi zat bereaksi
E. memperbesar luas permukaan zat pereaksi
Soal nomor 20
Reaksi dekomposisi sulfuril klorida adalah realski elementer : SO2(g) –> SO2(g) + Cl2(g).
Jika reaksi dimulai dengan [SO2Cl2] = 0,1 M dan laju awal reaksi adalah 2,2 x 10-6 M/s, pada saat [SO2] = 0,01 M, maka laju reaksinya adalah ….
A. 2,2 x 10-5 M/s
B. 1,98 x 10-5 M/s
C. 2,2 x 10-5 M/s
D. 1,98 x 10-5 M/s
E. 2,2 x 10-5 M/s
Soal nomor 21
Data hasil percobaan reaksi : 2X + 2Y –> Z pada volume 100 mL adalah sebagai berikut.
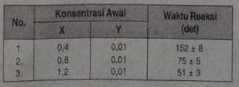
Orde reaksi terhadap X adalah ….
A. 0
B. 0,5
C. 1
D. 2
D. 3
Soal nomor 22
Cara praktis untuk menentukan laju reaksi : CaCO3(aq) + 2HCl(aq) –> CaCl2(aq) + H2O(l) + CO2(aq) adalah ….
A. laju pertambangan konsentrasi CaCO3
B. laju pertambangan konsentrasi HCl
C. laju pertambangan konsentrasi CaCl2
D. laju pertambangan konsentrasi CO2
E. laju pertambangan konsentrasi H2O
Soal nomor 23
Reaksi 2N2O5(g) ⇔4NO2(g) + O2(g) adalah reaksi eksoterm. Jika temperatur dinaikkan, yang terjadi adalah ….
A. NO2 dan O2 bertambah
B. N2O2 dan O2 bertambah
C. NO2 dan N2O5 berkurang
D. N2O5 dan O2 berkurang
E. NO2 dan O2 berkurang
Soal nomor 24
Pada reaksi setimbang :
| Fe3+(aq) + SCN–(aq) | ⇔ | Fe(SCN)2+(aq) |
| Tidak berwarna | Merah |
Apabila temperatur tetap dan jika ….
A. konsentrasi Fe3+ ditambah, warna larutan bertambah merah
B. larutan diencerkan, warna larutan bertambah merah
C. konsentrasi SCN– ditambah, warna larutan memudar
D. ke dalam larutan ditambahkan larutan amonia, warna larutan bertambah merah
E. ke dalam larutan ditambahkan suatu katalis, warna larutan memudar
Soal nomor 25
Di dalam volume 1 liter air dipanaskan gas NH3 sehingga terjadi reaksi berikut.
2NH3(g) ⇔ N2(g) + 3H2(g)
Data yang diperoleh sebagai berikut.
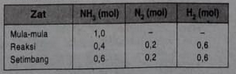
Harga kesetimbangan (Kc) dari data di atas adalah ….

Soal nomor 26
Perhatikan reaksi kesetimbangan berikut!
N2(g) + 3H2(g) ⇔2NH3(g)
Pada keadaan kesetimbangan terdapat tekanan parsial gas H2 = y dan NH3 = x atm. Jika harga Kp = 24, maka tekanan parsial gas H2 adalah ….

Soal nomor 27
Satu mol gas SO3 mula-mula terurai menjadi gas SO2 dan O2. Pada saat setimbang, SO3 terbentuk 0,4 mol. Besarnya derajat disosiasi (α) reaksi tersebut adalah ….
A. 0,3
B. 0,4
C. 0,5
D. 0,6
E. 0,7
Soal nomor 28
Di dalam bejana yang volumenya 2 liter terdapat kesetimbangan reaksi N2(g) + 3H2(g) ⇔ 2NH3(g). Pada keadaan setimbang, terdapat 2 mol N2, 4 mol H2, dan 8 mol NH3.
Harga konstanta kesetimbangan reaksi tersebut adalah ….
A. 0,5
B. 1
C. 1,5
D. 2
E. 2,5
Soal nomor 29
Di dalam volume 2 liter terjadi reaksi kesetimbangan 2SO3(g) ⇔2SO2(g) + O2(g).
Data yang diperoleh sebagai berikut.

Harga kesetimbangan (Kc) dari data di atas adalah ….
A. 10-8
B. 2 x 10-2
C. 5 x 10-2
D. 5 x 10-1
E. 2
Soal nomor 30
Di dalam reaksi 2SO3(g) ⇔2SO2(g) + O2(g) ternyata pada keadaan setimbang pada suhu tertentu terdapat 20% volume gas O2, Nilai derajat disosiasi pada reaksi tersebut adalah ….
A. 0,75
B. 0,60
C. 0,50
D. 0,35
E. 0,20
Kunci jawaban – Unduh
Demikian yang dapat kami bagikan mengenai contoh soal Penilaian Akhir Semester PAS Kimia kelas 11 K13 SMA MA tahun 2021. Semoga bermanfaat.



