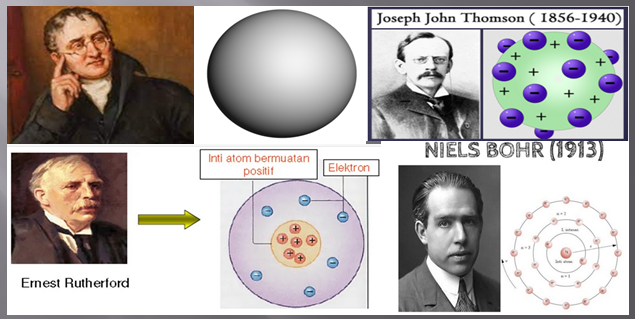
Struktur Atom : Nomor Atom, Nomor Massa, Isotop, dan Contoh Soalnya
Gurubagi.com. Semua atom dapat diidentifikasi berdasarkan jumlah proton dan neutron yang terkandung dalam atom tersebut.
Setiap atom memiliki nomor atom dan nomor massa, isotop, isobar dan isoton. Susunan atom satu dengan atom yang lain memiliki perbedaan yang jelas, baik jumlah proton, jumlah elektron maupun jumlah neutron.
Berikut ini adalah penjelasan mengenai nomor atom, nomor massa, dan isotop.
1. Nomor atom
Jumlah atom yang terdapat pada inti atom sama dengan nomor proton yang selanjutnya disebut sebagai nomor atom.
Untuk atom yang sama memiliki jumlah proton yang sama, akan tetapi berbeda dari atom unsur lain. Suatu atom netral memiliki jumlah elektron (e) yang sama dengan jumlah proton (p).
Nomor atom (Z) = jumlah proton (p) = jumlah elektron (e)
2. Nomor massa
Jumlah proton dan jumlah neutron dalam suatu atom disebut dengan nomor massa. Nomor massa sebuah atom hanya dapat ditentukan oleh banyaknya massa proton dan neutron. Massa elektron sangat kecil (kurang dari 1 atm), sehingga massa elektron dabaikan.
Nomor massa = (A) = jumlah proton (p) + jumlah neutron (n)
Nomor atom dan nomor massa dapat dinotasikan sebagai berikut.

Contoh Soal
Soal nomor 1
Tentukan jumlah proton, elektron, dan neutron dari atom oksigen berikut!
![]() dan
dan![]()
Pembahasan :
![]()
Unsur oksigen tersebut memiliki :
- Nomor masa, A = 16
- Nomor atom, Z = 8
Dengan demikian :
- Jumlah proton, p = Z = 8
- Jumlah elektron, e = Z = 8
Karena jumlah neutron, n = A – Z, maka n = 16 – 8 = 8, sehingga jumlah proton 8, jumlah elektron 8, dan jumlah neutron 8.
![]()
Unsur oksigen tersebut memiliki :
- Nomor Massa, A = 16
- Nomor Atom, Z = 8
- Muatan, m = -2
Dengan demikian :
- Jumlah Proton, p = Z = 8
- Jumlah Elektron, e = Z – m = 8 – (-2) = 8 + 2 = 10
Karena jumlah neutron, n = A – Z, maka n = 16 – 8 = 8, sehingga jumlah proton 8, jumlah elektron 10, dan jumlah neutron 8.
Soal nomor 2
Tentukan jumlah proton, elektron, dan neutron pada ion kalium bermuatan +1 berikut!
![]()
Pembahasan:
Unsur kalium tersebut memiliki :
- Massa, A = 39
- Atom, Z = 19
- Muatan, m = +1
Unsur tersebut memiliki:
- Jumlah proton, p = Z = 19
- Jumah elektron, e = Z – m = 19 – 1 = 18
Karena jumlah elektron, n = A – Z, maka n = A – Z = 39 – 19 = 20, sehingga jumlah proton 19, jumlah elektron 18, dan jumlah netron 20.]
Baca :
- Struktur Atom, Perkembangan Teori Atom, dan Partikel Penyusunnya
- Contoh Soal Kimia Struktur Atom Kelas 10 SMA MA dan Kunci Jawabannya
- Latihan Soal Struktur Atom Kimia Kelas 10 SMA MA dan Jawabannya
- Latihan Soal Struktur Atom Kimia Kelas 10 SMA MA Kurikulum 2013
- Contoh Soal Kimia Struktur Atom Kelas 10 SMA MA dan Kunci Jawabannya
- Contoh Soal Kimia Struktur Atom Kelas 10 SMA MA Kurikulum 2013
2. Isotop, Isoton, dan Isobar
a. Isotop
Isotop adalah atom-atom yang mempunyai nomor atom yang sama, akan tetapi memiliki massa atom yang berbeda, dengan unsur-unsur sejenis.
Contoh isotop:

b. Isobar
Isobar adalah atom-atom yang mempunyai nomor atom yang berbeda (nomor atom berbeda) namun memiliki massa atomnya sama.
Contoh isobar:

c.Isoton
Isoton, yaitu atom-atom unsur berbeda (nomor atom berbeda) yang mempunyai jumlah neutron yang sama.
Contoh isoton:

Contoh Soal
Tentukan pasangan pasangan unsur berikut yang merupakan isotop, isobar, isoton!

Pembahasan:

Demikian ulasan mengenai struktur atom (nomor atom, nomor massa, isotop) dan contoh soalnya. Semoga bermanfaat.